免职声明:本网站为公益性网站,部分信息来自网络,如果涉及贵网站的知识产权,请及时反馈,我们承诺第一时间删除!
This website is a public welfare website, part of the information from the Internet, if it involves the intellectual property rights of your website, please timely feedback, we promise to delete the first time.
电话Tel: 19550540085: QQ号: 929496072 or 邮箱Email: Lng@vip.qq.com
摘要:长庆气田的天然气净化厂主要生产单元包括脱硫单元、脱水单元和硫磺回收单元。(一)、脱硫单元1、天然气脱硫的原因和意义天然气中含有的H2S、CO2和有机硫等酸性组分,在水存在的情况下会腐蚀金属; 含硫组分有难闻的臭味、剧毒、使催化剂中毒等缺点。CO2为不可燃气..
|
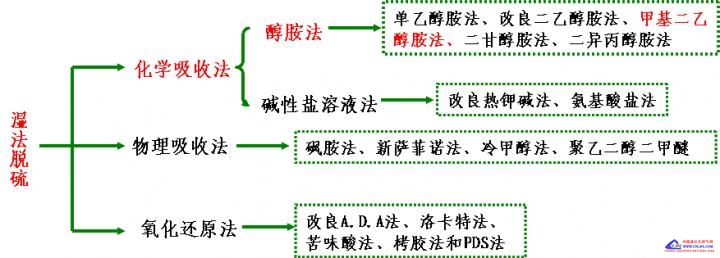
长庆气田的天然气净化厂主要生产单元包括脱硫单元、脱水单元和硫磺回收单元。 (一)、脱硫单元 1、天然气脱硫的原因和意义 天然气中含有的H2S、CO2和有机硫等酸性组分,在水存在的情况下会腐蚀金属; 含硫组分有难闻的臭味、剧毒、使催化剂中毒等缺点。CO2为不可燃气体,影响天然气热值的同时,也影响管输效率。特别是,H2S是一种具有令人讨厌的臭鸡蛋味,有很大毒性的气体。空气中H2S含量达到几十mg/m3就会使人流泪、头痛,高浓度的硫化氢对人有生命危险;H2S在有水及高温(400℃以上)下对设备、管线腐蚀严重;还对某些钢材产生氢脆,在天然气净化厂曾发生阀杆断裂、阀板脱落现象。有机硫中毒会产生恶心、呕吐等症状,严重时造成心脏衰竭、呼吸麻痹而死亡。 因此天然气脱硫有保护环境、 保护设备、管线、仪表免受腐蚀及有利于下游用户的使用等益处。 同时还可以化害为利,回收资源。将天然气中的硫化氢分离后经克劳斯反应制成硫(亮黄色,纯度可达99.9),可生产硫和含硫产品,在工业、农业等各个领域都有着广泛的用途。 从高含量CO2的天然气中分离出来的高纯度的CO2可用于制备干冰,也可用于采油上回注地层以提高原油的采收率。 2、天然气脱硫、脱碳的方法 关于天然气中酸性气体的脱除,开发了许多处理方法,这些方法可分成湿法和干法两大类。干法脱硫目前工业上已很少应用,工业大型装置以湿法为主。湿法脱硫按照溶液的吸收和再生方法,可分为化学吸收法、物理吸收法和氧化还原法三类。
2.1化学吸收法 化学吸收法是以可逆的化学反应为基础,以弱碱性溶剂为吸收剂,溶剂与原料气中的酸性组分(主要是H2S和CO2)反应而生成某种化合物;吸收了酸气的富液在升高温度、降低压力的条件下,该化合物又能分解而放出酸气。主要有代表醇胺法、改良热钾碱法、氨基酸盐法。 改良热钾碱法已成功地用于从气体中脱除大量CO2,也可用来脱除天然气中的CO2和H2S酸性气体。基本原理为: K2CO3+ CO2+H2O→2KHCO3 K2CO3+ H2S→2KHCO3+KHS 改良热钾碱法适用于含酸气量8%以上,CO2/H2S比高的气体净化。压力对操作影响较大,吸收压力不宜低于2MPa。 美国和日本合成氨厂很多采用这种方法脱CO2。美国装置数超过100套,日本装置数超过500套。 2.2物理吸收法 物理吸收法是基于有机溶剂对原料气中酸性组分的物理吸收而将它们脱除,溶剂的酸气负荷正比于气相中酸性组分的分压。富液压力降低时,随即放出所吸收的酸性组分。物理吸收一般在高压和较低的温度下进行。 物理吸收法的主要代表有冷甲醇法、碳酸丙烯酯法、N-甲基吡咯烷酮法、聚乙二醇二甲醚法和磷酸三丁酯法。 物理吸收法具有如下特点: 1) 一般在高压和较低的温度下进行; 2) 溶剂酸气负荷高,适宜于处理酸气分压高的原料气; 3) 溶剂不易变质,腐蚀性小,能脱除有机硫化物; 但物理吸收法不宜用于重烃含量高的原料气,且受溶剂再生程度的限制,净化率较化学吸收法低。 ① 冷甲醇法 冷甲醇法是以甲醇为吸收剂,在低温(低于-50℃)下吸收酸性气体的物理吸收法。 甲醇在高压低温下CO2和H2S有很高的溶解度,适宜于酸气分压大于1.0MPa的原料气,可选择性地脱除H2S并可同时脱除有机硫化物。 ② 聚乙二醇二甲醚法 聚乙二醇二甲醚法(Selexol法)用聚乙二醇二甲醚作溶剂,旨在脱除气体中的CO2和H2S。由于聚乙二醇二甲醚具有吸水性能,因而该法还能同时产生一定的脱水效果。 2.3化学―物理吸收法 化学―物理吸收法是一种将化学吸收剂与物理吸收剂联合应用的酸气脱除法,目前以环丁砜法为常用。物理吸收溶剂是环丁砜,化学吸收溶剂可以用任何一种醇胺化合物,但常用的是二异丙醇胺(DIPA)和甲基二乙醇胺(MDEA)。 2.4湿式氧化法 这类方法的研究始于本世纪二十年代,至今已发展到百余种,其中有工业应用价值的就有二十多种。主要湿式氧化法有改良的ADA法 (蒽醌法)、 螯合铁法、 PDS法。 湿式氧化法具有以下特点: 1) 脱硫效率高,可使净化后的气体含硫量低于 5.0 mg/m3; 2) 可将H2S转化为单质疏,无二次污染; 3) 可在常温和加压状态下操作; 4) 大多数脱硫剂可以再生,运行成本低。 2.5 干法脱除酸性气体 所谓干法,是应用固体材料吸附、化学反应、气体分离等技术脱除天然气中H2S和CO2组分。干法主要包括氧化铁法、活性炭法、分子筛、膜分离法等。 干法脱除酸气技术通常用于低含硫气体处理,特别是用于气体精细脱硫。大部分干法脱硫工艺由于需要更换脱硫剂而不能连续操作,还有一些干法如锰矿法、氧化锌法等,脱硫剂均不能再生,脱硫饱和后要废弃,一方面会造成环境问题,另一方面会增加脱硫成本。 ① 氧化铁法 氧化铁法是用氧化铁(即人们熟知的海绵铁)脱H2S,是一种古老而知名的气体脱硫方法,迄今仍在许多特殊用途的领域中广泛应用。 ②分子筛法 分子筛对极性分子的吸附选择性,对硫化物产生了高的容量。由于它对有机硫化物,同对硫化氢一样具有很大的化学亲合力,因此,分子筛不仅可以除去H2S,而且对CS2、硫醇等其它含硫化合物也有较好的去除效率,处理后气体硫含量降至0.4 ppm(0.53 mg/m3)以下。现在,美国已经有多个工业分子筛装置在运转。 3、甲基二乙醇胺、二乙醇胺的脱硫、脱碳原理 醇胺类化合物(MEA、DEA、MDEA等)中至少含有一个羟基(OH)和一个胺基(NH2)。羟基的作用是降低化合物的蒸汽压,并增加在水中的溶解度;而胺基则为水溶液提供必要的碱度,促进酸性组分的吸收。 天然气脱酸性气体常用的醇胺有一乙醇胺(MEA)、二乙醇胺(DEA)、二甘醇胺(DGA)、二异丙醇胺(DIPA)、甲基二乙醇胺(MDEA)等。 3.1 一乙醇胺(MEA) MEA是工业用醇胺中的碱性最强的,它与酸性组分迅速反应,能容易地使原料气中H2S含量降到5mg/m3以下。它既可脱H2S,也可脱CO2,一般情况下对两者无选择性。MEA在醇胺中相对摩尔质量最小,因而以单位重量或体积计具有最大的酸气负荷。 3.2 二乙醇胺(DEA) DEA和MEA的主要区别是它与COS及CO2的反应速度较慢,因而DEA与有机化合物反应而造成的溶剂损失量少。对有机硫化物含量较高的原料气,用DEA脱硫较有利。DEA对CO2 对H2S也没有选择性。 3.3甲基二乙醇胺(MDEA) MDEA是用于天然气脱硫的烷醇胺类化合物中受到普遍关注的一种溶剂。该法在五十年代初就已通过工业放大试验,被证实具有对H2S优良的选择脱除能力和抗降解性强、反应热较低、腐蚀倾向小、蒸气压较低等优点。 长庆气田目前使用的脱硫溶剂主要有甲基二乙醇胺(MDEA)和二乙醇胺(DEA)。这两种溶液在工业上广泛使用。主要的物理化学性质见下表:
3.4甲基二乙醇胺和二乙醇胺脱硫、脱碳原理 甲基二乙醇胺的化学分子式 :
CH2CH2OH 主反应: H2S+R3N === R3NH++HS- (瞬间反应) CO2+R3N (不反应) 副反应: CO2+H2O === H++HCO3- (极慢反应) R3N + H + === R3N H + (瞬间反应) R3N + H2O === R3NH ++ OH- (慢反应) 二乙醇胺的化学分子式:
CH2CH2OH
主反应: 2R2NH+H2S=== (R2NH)2S (瞬间反应) 2R2NH+H2O+CO2 ===(R2NH2)2CO3 副反应: (R2NH2)2CO3+H2O+CO2 === 2R2NH2HCO3 2R2NH +CO2=== R2NCOONH2R2 (R2NH)2S+H2S === 2R2NHHS MDEA和CO2的反应速率较慢,对H2S有较好的选择吸收性,单一的MDEA溶液较难深度脱除天然气中的CO2,加入DEA可加快溶液与CO2的反应速率,达到深度脱除CO2的目的,使净化气中满足CO2含量<3%的要求。二乙醇胺(DEA)为仲胺,碱性较强,经过试验筛选,靖边气田净化厂的复合溶液中甲基二乙醇胺溶液一般浓度为40%,二乙醇胺溶液的浓度控制在5%左右 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||